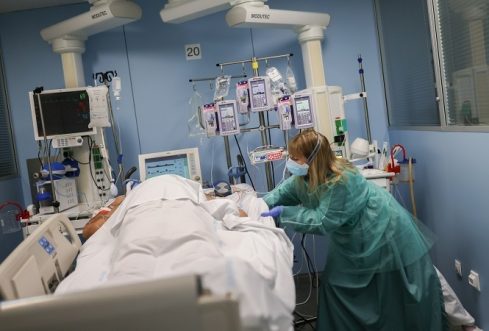
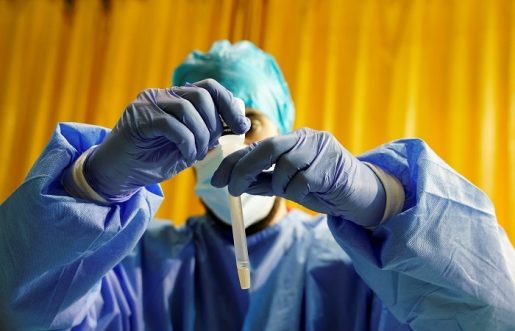
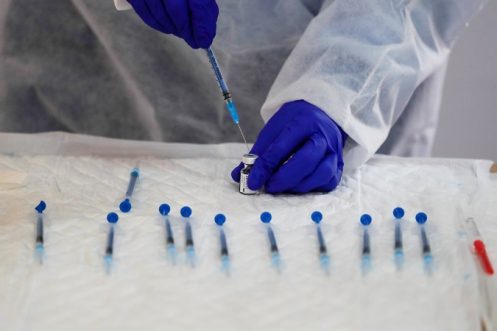
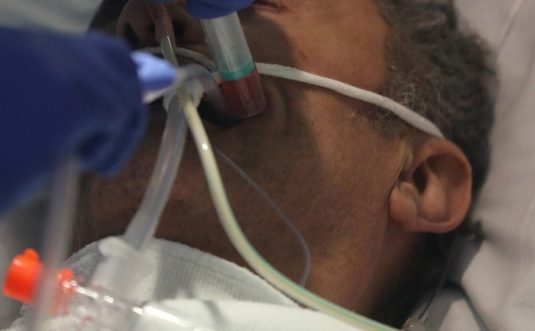
Luis Enjuanes, Centro Nacional de Biotecnología (CNB – CSIC)
Luis Enjuanes vive a contrarreloj desde que comenzó la pandemia. A sus 76 años, lidera un equipo de 16 personas cuyo objetivo es terminar la que podría ser una de las mejores vacunas contra el SARS-CoV-2. Por varias razones: Es autoamplificable, lo que significa que la dosis de ARN que se inyecta puede multiplicarse 5 000 veces dentro del organismo. Genera una inmunidad esterilizante, es decir, las personas vacunadas no solo no enferman, sino que tampoco se infectan ni transmiten el virus. Su administración podría ser intranasal, lo que da mayor protección en las vías respiratorias, la principal puerta de entrada del coronavirus.
Enjuanes, que desarrolla su actividad en el Centro Nacional de Biotecnología (CNB-CSIC), prevé que su vacuna estará lista en un año. “Saldremos más tarde, pero con todo actualizado”, afirma. Se refiere a que en los ensayos han incorporado las mutaciones de las variantes del SARS-CoV-2 de Reino Unido, Sudáfrica y Brasil.
Más allá de su investigación, el virólogo explica por qué este coronavirus es más letal que otros, augura nuevas epidemias y cambios en nuestro modo de vida, y da por hecha la irrupción de las vacunas españolas en la lucha contra la covid-19. Nada más empezar, advierte: “Ahora no podemos bajar la guardia”.
Después de un año de pandemia, ¿cómo valora el momento actual?
Estamos en un momento relativamente optimista. Hay tres vacunas que ya se administran y la UE acaba de aprobar la de Janssen. Esto es lo más importante: la vacunación es la única forma frenar la pandemia de forma masiva. Las vacunas de Pfizer, Moderna y AstraZeneca son efectivas, pero no perfectas: hay que dar dos dosis y la gente vacunada, aunque está protegida de sufrir una patología intensa y morir por covid-19, también se infecta y puede diseminar el virus. Hay que llegar al 70 % de la población inmunizada. Las cifras han bajado, pero ahora no podemos bajar la guardia y dilapidar la labor que la mayoría de la población y las instituciones están realizando. Si esperamos 2 o 3 meses más, solucionaremos el problema. Con el 70 % vacunado, el virus se extingue de forma natural: cuando va a infectar a una persona, fracasa en el 70 % de los casos.
Además de cierto optimismo, la vacunación está generando interés respecto a las 3 vacunas que se desarrollan en el CSIC. ¿En qué fase está la suya? ¿Cuándo estará finalizada?
La nuestra es una vacuna original, no se ha hecho ninguna de este tipo. Está basada en la manipulación genética del propio SARS-CoV-2, del que hemos derivado un replicón de ARN [que multiplica la dosis génica que desencadena la protección]. Esa parte ya está definida, pero necesitamos tecnologías complementarias para la administración de la vacuna. Tenemos que combinar ambas cosas y comprobar que todo funciona, que la vacuna es estable y segura. De aquí al verano realizaremos los ensayos con ratones y hámster. Si todo va bien, haremos lo mismo con macacos. Creo que estará lista en el primer trimestre de 2022. Entonces habremos obtenido datos de ensayos clínicos para probar la seguridad de la vacuna y poder administrarla entre la población. Nos gustaría ir más deprisa, pero es un modelo nuevo y requiere tiempo.
Nos cuesta entender los ritmos de la ciencia, aunque precisamente lo que más nos preocupa es la seguridad de las vacunas. Y para garantizarla es necesario realizar sucesivos experimentos con animales y ensayos clínicos en humanos.
Así es. Generalmente, una vacuna tarda entre 10 y 15 años en desarrollarse. Ahora las multinacionales están trabajando con equipos de unas 600 personas, grandes instalaciones y muchos recursos económicos para ir más rápido. A nosotros no nos ha faltado financiación en estas primeras fases, y tanto el CSIC como el Ministerio de Ciencia nos apoyan mucho, pero tenemos que completar la investigación para una vacuna nueva. Otras, como la de AstraZeneca o la que desarrolla Mariano Esteban, se basan en vectores conocidos y por tanto aprobados por las agencias reguladoras de medicamentos. Eso les permite correr más. Nosotros, antes de hacer la vacuna contra el SARS-CoV-2, ya habíamos desarrollado otra [similar] para el virus MERS que era muy eficaz en los modelos animales experimentales. Inducía una inmunidad esterilizante: cuando inmunizamos a ratones humanizados [modificados genéticamente] y tratamos de infectarlos 3 semanas después, el virus no podía entrar porque estaban muy bien protegidos. Eso no ocurre con las otras vacunas.
Digamos que por un lado está el corazón de la vacuna, que ustedes ya han diseñado a partir de la ingeniería genética, y por otro la tecnología que facilita su administración, una especie de cápsulas que cubren el ARN para que no se degrade y pueda penetrar en las células.
Exactamente. Esos recubrimientos pueden ser de distinta naturaleza y ya están fabricados, pero hay que combinarlos con el corazón de la vacuna, lo que lleva la maquinaria de amplificación del ARN que provoca la expresión de proteínas que inducen protección. Al combinarlos, queremos ver cuál es el método más efectivo. Por ejemplo, las vacunas de Moderna y Pfizer, basadas en moléculas de ARN mensajero, necesitan conservarse a 20 grados bajo cero; sin embargo, la compañía alemana CureVac se ha aliado con Bayer para sacar otra vacuna de ARN mensajero a la que han añadido un excipiente que hace que pueda almacenarse a 4 grados en el frigorífico de casa. Moderna y Pfizer acabarán hablando con CureVac para que les traspase esa tecnología. Lo que quiero decir es que no solo estamos haciendo una vacuna, sino casi 30 variantes para seleccionar el prototipo más seguro y eficaz.
Su vacuna se basa en un replicón sintético de ARN, algo intermedio entre las vacunas de Pfizer y Moderna, que son sintéticas, y las que se basan en virus, o sea, organismos vivos.
Sí. Tenemos dos versiones y ambas se basan en el mismo replicón, derivado del genoma del virus, al que hemos quitado una colección de genes. Como resultado, ya no es un virus porque no se puede propagar e ir infectando a personas o animales. Eso nos da la seguridad de que no va a revertir a una entidad virulenta. Llevamos muchos años trabajando en vacunas y sabemos que hay muchas basadas en virus vivos atenuados que funcionan muy bien. Pero como los virus se reproducen a una gran velocidad, existe la posibilidad de que alguno logre hacerse virulento. Además, nuestra vacuna incluye un ARN muy grande que lleva el ‘motor’ para autoamplificarse: si damos 1 microgramo, una vez que entra en las células del cuerpo humano, puede ‘fabricar’ entre 1 000 y 5 000. Eso tampoco lo hacen las de Moderna o Pfizer.
¿Cómo se administrará su vacuna?
Hemos utilizado una ruta de administración intranasal, pero las agencias que controlan la seguridad de los medicamentos prefieren la intramuscular, que se ha usado más y es segura. Sin embargo, no es la más adecuada porque induce una inmunidad general en todo el organismo, sistémica, y menos fuerte en las mucosas. Las mucosas (nasales, oculares, respiratorias, etc.) son espacios abiertos al exterior y la inmunidad en esas zonas se induce mejor localmente, presentando ahí el antígeno [la sustancia que provoca la respuesta inmunitaria; en este caso, la vacuna]. Este virus entra prioritariamente en nuestro organismo a través de las vías respiratorias, por eso si administras la vacuna intranasalmente, inmunizas esa zona y la protección es mayor. Esto lo vimos con el prototipo vacunal que desarrollamos para el MERS que vino de Oriente Medio; su eficacia era muy alta porque generaba una inmunidad fuerte. A cambio, hay que hacer más ensayos para demostrar la seguridad. Tenemos dos vías de administración en estudio: la intranasal y la intramuscular, que se inyecta en un brazo. Varias compañías que han fabricado vacunas intramusculares están investigando vías para administrarlas intranasalmente –con sprays– de forma segura. Nosotros vamos a por una vacuna intranasal y de una sola dosis muy potente.
¿Existen otras vacunas contra la covid-19 que sean autoamplificables? Esta característica, además de aumentar su eficacia, ¿qué otras ventajas aporta?
Ya he dicho que esto implica que el propio sistema puede multiplicar entre 1 000 y 5 000 veces la dosis de ARN que das al principio. Por tanto, se necesitaría una cantidad inicial mucho menor y el coste se reduciría. Los científicos de Moderna y Pfizer lo saben, pero han optado por ir deprisa y la primera versión de vacuna que han sacado no es autoamplificable. Ahora están trabajando en otras que lleven una maquinaria de autoamplificación sencilla para realizar los controles rápidamente. En contraste, la nuestra lleva el propio motor del virus y amplifica no solamente uno sino varios de sus genes. No se centra solo en el gen de la proteína S de las espículas –la más importante para inducir la protección–, también en los de otras como la nucleoproteína, que favorece una respuesta celular a través de los linfocitos T. Estos destruyen las células del organismo que han sido infectadas, entonces el virus sale al exterior y es neutralizado por los anticuerpos. Así logramos una inmunidad más amplia y potente.
En algún medio se ha afirmado que su vacuna podría estar entre las mejores del mundo. Recapitulemos, ¿cuáles son sus puntos fuertes frente a otras?
En primer lugar, como acabo de decir, no utiliza un solo antígeno para inmunizar, sino varios del propio virus. Segundo, al ser autoamplificable puede multiplicar hasta 5 000 veces la dosis inicial. Tercero, el uso de la vía intranasal aumenta su potencia porque induce inmunidad en las mucosas respiratorias, que se distingue de la inmunidad sistémica en que genera gran cantidad de inmunoglobulinas del isotipo IgA. Hay varias clases de anticuerpos. Los IgM son los primeros que se fabrican pero decaen enseguida. Luego se generan los IgG, que son de larga duración. Pero en las mucosas se producen además los anticuerpos IgA, que muestran una particularidad: tienen cuatro sitios de unión para agarrar al virus. Cuando se unen al virus, este ya no puede soltarse, queda neutralizado. Por eso estas inmunoglubulinas IgA son más potentes, y también porque, como se han seleccionado para trabajar en medios exteriores como las mucosas respiratorias o entéricas, su naturaleza es más estable frente a la degradación. A diario ingerimos alimentos de diversa procedencia que traen muchos contaminantes; necesitamos tener una inmunidad muy potente a lo largo del intestino. Ese tracto degrada todo lo que comemos, pero también los anticuerpos, por eso es esencial que tengamos IgA tetravalentes que se unan al virus con una avidez muy alta.
¿Existe alguna vacuna que aúne estas características?
En funcionamiento, no. Pero muchas empresas ya están fabricando vacunas autoamplificables y que se administren vía intranasal. Aunque ninguna ha sido aprobada aún, no tardarán mucho en lograrlo, porque eso abarata costes y hace que sean más efectivas. Estas tecnologías se conocen y ya hay varios prototipos. Más que tecnológico, diría que el problema es lograr la aprobación, hacer productos seguros.
Ha explicado que su vacuna es autoamplificable y genera inmunidad esterilizante. Hay dos preguntas que siguen siendo cruciales: cuánto durará esa inmunidad y hasta qué punto será una vacuna eficaz frente a las nuevas cepas o variantes del virus
Al basarse en un ARN autorreplicante, induce una inmunidad no solo de alto nivel, también de larga duración. En principio nuestra vacuna debería ser más inmunogénica que las que se están suministrando ahora, porque además incluye varias proteínas del virus. Ahora bien, esa duración, para cualquier vacuna que induzca una inmunidad en las mucosas respiratorias, puede ser de 1, 2 o como máximo 3 años. Antes comparaba la inmunidad en mucosas con la sistémica, la que dan las vacunas contra el virus de la polio, el sarampión o la viruela. Esa puede durar 20, 30 o 40 años con una sola dosis. El asunto de las nuevas variantes lo tenemos controlado. La versión en la que nos estamos centrando incluye las mutaciones de los virus del Reino Unido, Sudáfrica y Brasil, y seguramente también de alguna variante de Estados Unidos que ha aparecido en California y Nueva York. Saldremos más tarde, pero con todo actualizado. En todo caso, si esto sigue así, habrá que actualizar las vacunas cada año, como sucede con el virus de la gripe, en función de las variantes que surjan.
REUTERS/Sergio Perez
Alguna vez ha afirmado que el SARS-CoV-2 es muy diferente a otros coronavirus –solo se conocen 7 que infecten a humanos– y que usted mismo preveía que a estas alturas ya estaría atenuado. Sigue desconcertando la disparidad de reacciones que causa: algunos organismos enferman hasta el punto de morir y en otros la sintomatología es muy leve o inexistente.
Las razones de la gravedad de este virus son múltiples, pero destaco una: normalmente los virus son específicos de un tejido, es decir, un virus hepático produce un tipo de infección en el hígado. El SARS 1, el coronavirus de 2002, básicamente infectaba el tracto respiratorio y el tracto entérico. En general, cuando un coronvairus contagia a una célula, se une a ella, pero no entra en su interior; la proteína S de las espículas tiene que cortarse en dos sitios para que cambie su estructura, se active y penetre en la célula. Con el SARS 1, ese corte solo se podía hacer en el pulmón o en el intestino, por eso infectaba esos tejidos. Pero debido a la inserción de 4 aminoácidos en la proteína S de las espículas, ahora se puede cortar por una enzima (la furina) que está en todos los órganos del cuerpo: pulmones, tracto intestinal, corazón, cerebro, venas, hígado, riñón, páncreas… El SARS-Cov-2 tiene lo que se llama un politropismo, puede infectarte cualquier órgano. Por eso causa como poco 50 patologías distintas.
¿Ese inserto se ha producido por una mutación del virus?
Lo correcto es decir ‘inserción’, que significa que ha adquirido un nuevo componente de otro virus o de una célula. Lo ha incorporado y por eso puede causar una variedad de patologías. Los pacientes hospitalizados suelen estar infectados en varios órganos. Este virus causa diarrea, trastornos del sistema nervioso y el comportamiento, problemas en la boca que hacen que pierdas el gusto y el olfato, trastoca el sistema circulatorio porque afecta a las células endoteliales de las venas… Y encima tiene la capacidad de infectar de forma silenciosa. A veces no te das cuenta porque no tienes fiebre, ni problemas respiratorios, ni ningún síntoma; sigues con tu vida normal y vas diseminando el virus. Esa combinación hace que sea tan mortal.
Además, hay aspectos que generan mucha confusión. Por ejemplo, entre la gente que se ha infectado, la evolución de los anticuerpos es muy dispar. Y entre quienes desarrollan la enfermedad, no está claro hasta cuándo pueden seguir contagiando tras la recuperación.
Yo he hablado personalmente con José Ramón Arribas, jefe del servicio de enfermedades infecciosas del hospital de la Paz, y Rafel Delgado, director del servicio de microbiología del Hospital 12 de Octubre. Ambos están al pie del cañón y conocen muy bien la variedad de patologías que produce el virus. Su vasto conocimiento lo resumiré diciendo que las analíticas de las personas infectadas son supervariables. Algunas se infectan y enseguida enferman gravemente, otras se infectan y son asintomáticas; las hay que inducen muchos anticuerpos, frente a otras que no; hay personas que además de inducir muchos anticuerpos, les duran tiempo, mientras que en otras estos desaparecen en unas semanas. Se dan todas las combinaciones imaginables. Hay personas que se infectan, enferman y se recuperan, mientras que otras permanecen infectadas 3, 4 o 5 meses. Puede pasar cualquier cosa.
Eso también dificulta el control de la pandemia.
Por supuesto. Por eso los médicos, ante alguien con dos o tres PCRs negativas, suelen decir: ‘Váyase a casa, pero siga usando la mascarilla, tenga muchas precauciones y en unas semanas venga a hacerse otra analítica’. Hay que inculcar esa cultura de la precaución. Cuando una persona aún muestra carga viral, pero al mismo tiempo ha desarrollado muchos anticuerpos, se le pide que tenga cuidado, aunque ya vaya a trabajar porque no suele transmitir. En esto no sirven las afirmaciones rotundas, no todo es blanco o negro. A veces hay que dar normas de conducta genéricas, pero cada uno tenemos una genética y un sistema inmunitario.
Dentro de la comunidad científica, no es el único que augura otra pandemia en 4 o 5 años.
Pero con un matiz: una pandemia es una infección de alcance mundial, como esta, que se ha extendido a 192 países. Lo que afirmo es que habrá epidemias restringidas a 2, 3, 5 países… Las estadísticas dicen que cada uno o dos años aparece un nuevo coronavirus o reaparece uno ya conocido en animales. En humanos surge uno nuevo cada 6-8 años, que puede ser incluso mortal, como el SARS-CoV-2. Pero afortunadamente no todo son pandemias universales, como esta o la de la gripe de 1918. Solo aseguro que volverá a haber epidemias de este u otros virus. Ahora la OMS está prediciendo un brote de Nipah, un virus que traen los murciélagos. Lo que ha sucedido en el pasado seguirá pasando incluso con más intensidad; ahora los sistemas de transporte nos permiten estar en las antípodas en 24 horas, la densidad de la población ha aumentado muchísimo, y accedemos a espacios que antes eran inaccesibles.
Desde hace un año, vivimos en una especie de carrera por las vacunas que tiene tintes geopolíticos. ¿España estará en lo que sería la segunda ola de vacunas?
Es muy probable que la que desarrolla mi colega Mariano Esteban, que usa un vector viral con el que ya han fabricado 7 vacunas, esté lista para esa segunda ola a finales de año. La de Vicente Larraga va bastante avanzada y es fácil de producir, así que podría ser la segunda. La nuestra, si todo va bien, será la tercera, pero no estará lista antes de principios de 2022.
A raíz de esta pandemia, ¿tendrá la ciencia un mayor protagonismo en la esfera política?
Se está reflexionando mucho sobre esto porque la pandemia ha puesto la salud global en peligro, ha causado gran impacto socioeconómico, los medios de comunicación están volcados en su evolución… Lógicamente, quienes toman las decisiones políticas lo hacen de acuerdo con las urgencias y necesidades creadas por la crisis. Me consta que en España se están haciendo verdaderos esfuerzos por impulsar la ciencia y prepararnos mejor para otras epidemias o pandemias, a través de métodos de diagnóstico precoz, investigación en antivirales, inmunoterapias y nuevas vacunas. Sí, creo que esto va a suponer un antes y un después, aunque, como ocurre siempre, decaerá el momentum actual.
¿Cree que hasta cierto punto esta crisis nos va a cambiar la manera de vivir?
Creo que sí. Ha afectado mucho a nuestro modo de vida, a la vida familiar y social, al ocio… La gente se va a volver más precavida. Hemos aprendido que con el uso de la mascarilla, la desinfección de manos y el mantenimiento de la distancia de seguridad disminuyen drásticamente las infecciones por gripe y otras. Llevar mascarilla va a ser más frecuente entre quienes viajen en medios de transporte o vayan a lugares de gran afluencia, sobre todo en determinadas etapas del año en las que aparecen los virus estacionales. Yo pienso utilizarla más a menudo en algunos espacios públicos. Creo que el segmento de la población que es más prudente va a cambiar sus hábitos de vida significativamente.
¿En qué ha cambiado su vida en el último año?
R: Me ha cambiado mucho. Yo estaba empezando a reducir mi actividad científica, pero para los que somos especialistas en coronavirus resultaba duro abandonar el barco en estas circunstancias. Por eso seguimos trabajando. He extendido mi periodo como ad honorem hasta que vea que la situación está encarrilada y que la dirección del laboratorio queda en buenas manos. Las 16 personas que lo configuramos estamos trabajando al máximo. Esta situación nos ha reunido a todos en torno a un proyecto central: la obtención de la vacuna.
Esta entrevista realizada por Mónica Lara del Vigo fue publicada en la web del CSIC.
Luis Enjuanes, director del laboratorio de coronavirus del CNB-CSIC, Centro Nacional de Biotecnología (CNB – CSIC)
Este artículo fue publicado originalmente en The Conversation. Lea el original.
Lea también en Cambio16.com: