En un hito histórico, un equipo de médicos y científicos de la Facultad de Medicina de Harvard y el Hospital General de Massachusetts lograron un avance revolucionario: el primer trasplante de un riñón de cerdo genéticamente modificado a un humano. Fue posible siete décadas después de que el primer trasplante de riñón del mundo se realizara en el Brigham & Women’s Hospital.
El procedimiento es conocido como xenotrasplante. Los investigadores han estado explorando el xenotransplante como una posible solución a la creciente escasez de órganos donados. La Red Unida para la Compartición de Órganos estima que más de 100.000 personas en Estados Unidos están en la lista de espera para un trasplante de órgano y 17 personas mueren cada día sin lograrlo.
Los riñones son los órganos más demandados, como se refleja en el Journal of the American Society of Nephrology. Pacientes que necesitan un nuevo riñón o deben someterse a diálisis para filtrar los residuos de la sangre. En sesiones largas y dolorosas que pueden durar varias horas, varias veces a la semana. El avance en el xenotrasplante podría ser un rayo de esperanza.
Cuatro horas en el quirófano
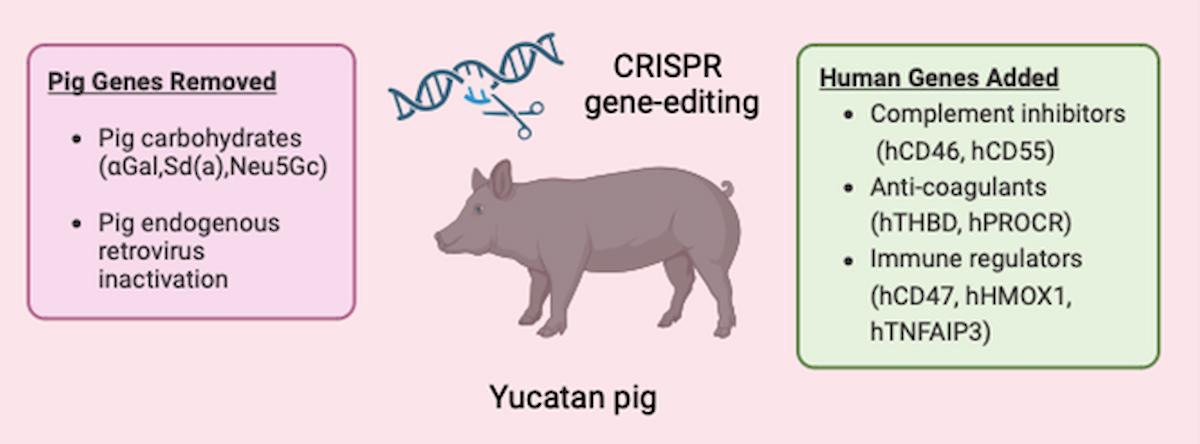
Richard (Rick) Slayman, un residente afroamericano de 62 años de Weymouth, Massachusetts, se convirtió en el primer humano en recibir un riñón de cerdo genéticamente modificado. La operación, que tuvo lugar el 16 de marzo, duró cuatro horas. El riñón de cerdo fue modificado genéticamente para ser más compatible con los humanos. Los científicos utilizaron la tecnología de edición genética CRISPR-Cas9 para eliminar genes porcinos específicos, añadir genes humanos y desactivar ciertos virus en el genoma porcino. En total, se realizaron 69 modificaciones genéticas en el riñón.
El riñón modificado fue proporcionado por eGenesis, una empresa de terapias de xenotrasplante cofundada por el genetista George Church y el antiguo becario postdoctoral Luhan Yang. Durante los últimos cinco años, eGenesis y Mass General han llevado a cabo una extensa investigación. Slayman también recibió nuevos medicamentos de anticuerpos monoclonales diseñados para suprimir las reacciones inmunitarias contra el tejido porcino. Antes de la operación, los órganos y los medicamentos inmunosupresores se probaron exhaustivamente en modelos animales para desarrollar un protocolo óptimo para su uso en humanos
El equipo quirúrgico que realizó la operación de trasplante estuvo integrado por 15 personas, y dirigido por el Dr. Tatsuo Kawai y el Dr. Nahel Elias. Cuando el riñón comenzó a producir orina, el equipo en el quirófano aplaudió. “Era realmente el riñón más bonito que he visto nunca”, dijo Kawai. Casi una semana después de la operación, Slayman se está recuperando bien y se espera que sea dado de alta pronto, según el equipo de Mass General.
El valiente Slayman
Según el equipo médico el verdadero héroe de es el paciente, el Sr. Slayman. El éxito de esta cirugía pionera, antaño considerada inimaginable, no habría sido posible sin su valentía y su voluntad de embarcarse en un viaje a un territorio médico inexplorado. Richard “Rick” Slayman, es director de sistemas del Departamento de Transportes de Massachusetts. Después de que sus riñones fallaran, estuvo en diálisis durante siete años y finalmente recibió un riñón humano en 2018.
Sin embargo, el órgano donado falló cinco años después y desarrolló otras complicaciones, incluida la insuficiencia cardíaca congestiva. Cuando Slayman reanudó la diálisis en 2023, experimentó graves complicaciones vasculares y necesitó hospitalización recurrente. A pesar de sus problemas de salud, Slayman continuó trabajando y se enfrentó a una larga espera, de entrre 4 a 5 años, para recibir otro riñón humano.
Cuando el Dr. Winfred Williams le planteó la posibilidad de recibir un riñón de cerdo, Slayman tuvo muchas dudas, pero finalmente decidió proceder. Vio esta oportunidad no solo como una forma de ayudarse a sí mismo. También como una forma de dar esperanza a miles de personas que necesitan un trasplante para sobrevivir. El avance puede tener un impacto significativo en los pacientes negros, quienes sufren altas tasas de insuficiencia renal terminal.
Nuevo fármaco
También Eledon Pharmaceuticals logró un hito médico con la realización exitosa de la operación. El anticuerpo anti-CD40L, Tegoprubart, jugó un papel crucial en el régimen de tratamiento inmunosupresor. Ayudando a prevenir el rechazo del órgano trasplantado por el cuerpo del paciente. El uso de Tegoprubart es parte de los esfuerzos para proporcionar nuevas opciones a los pacientes que necesitan trasplantes de órganos en medio de una escasez mundial de órganos disponibles.
Los fármacos fueron proporcionados sin costo alguno por dos empresas farmacéuticas. «Esta colaboración entre el mundo académico y la industria es crucial para avances como el que compartimos hoy», afirmó Leonardo Riella, catedrático asociado de cirugía de HMS Harold y Ellen Danser y director médico de trasplantes renales del Mass General.
Eledon participó previamente en procedimientos de trasplante de riñón y corazón con Tegoprubart, que se ha observado seguro y bien tolerado en múltiples estudios. La empresa también está llevando a cabo estudios preclínicos y dos ensayos clínicos globales centrados en la prevención del rechazo de órganos en receptores de trasplantes de riñón.
En un reciente estudio de fase 1b con 11 participantes, Tegoprubart demostró ser seguro y generalmente bien tolerado, previniendo eficazmente el rechazo y permitiendo una función renal postrasplante superior a las medias históricas. Actualmente, la empresa está reclutando participantes para el estudio de fase 2 BESTOW, que compara Tegoprubart con tacrolimus, un tratamiento estándar actual para la prevención del rechazo. Se espera completar la inscripción para este estudio a finales de 2024.
Seguimiento
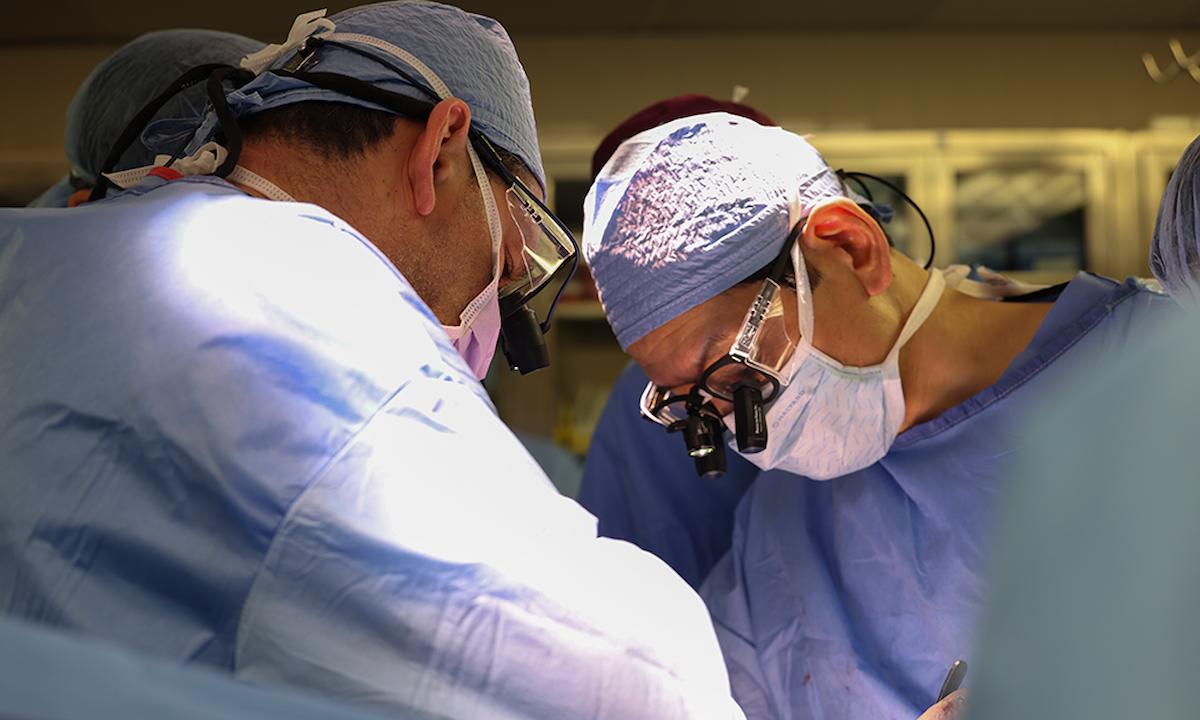

La operación de Slayman se realizó bajo un protocolo de la Administración de Alimentos y Medicamentos conocido como disposición de uso compasivo, que se otorga a pacientes con enfermedades potencialmente mortales que podrían beneficiarse de un tratamiento no aprobado. El Dr. Tatsuo Kawai, quien lideró el trasplante, espera que el riñón funcione durante al menos dos años. Si falla, Slayman podría volver a la diálisis.
Hasta ahora, el nuevo riñón de cerdo parece estar funcionando bien. Produce orina y filtra la creatinina, un producto de desecho. Los médicos seguirán vigilando a Slayman en busca de signos de rechazo del órgano. El equipo espera que el riñón de cerdo mejore la salud del paciente y le dé tiempo para recibir quizá otro riñón humano donado. Según el comunicado del Mass General la operación se considerará un éxito si no necesita volver a someterse a diálisis.
Miles en espera
De los 36 millones de estadounidenses afectados por enfermedades renales crónicas, unos 800.000 padecen insuficiencia renal terminal. La cual que es tres veces más común entre los estadounidenses de raza negra que entre los de raza blanca. Condición que requiere un nuevo riñón o sesiones de diálisis que pueden durar varias horas seguidas, varias veces a la semana. Aunque la diálisis puede mantener con vida a las personas, el tratamiento ideal es el trasplante de órganos.
Pero, la escasez de órganos es grave. En EE. UU. la lista de espera para recibir un riñón trasplantado de un donante humano vivo o fallecido supera las 100.000 personas. Pero solo se realizan 25.000 trasplantes de riñón al año. Mientras que en Europa más de 87.000 pacientes esperan por un trasplante. En 2022 en el mundo se realizaron apenas 157.540 trasplantes de órganos en 91 países.
Diálisis opción mala y cara
La demanda mundial de órganos humanos supera con creces la oferta, a pesar de los criterios restringidos de elegibilidad de órganos y la amplia elegibilidad de los donantes. En 2022, solo había 14.905 donantes fallecidos en EE. UU. y 6.466 donantes vivos. Actualmente, la lista de espera de Estados Unidos para trasplantes de riñón está aumentando en alrededor de 14.000 pacientes por año.
La diálisis sigue siendo la única opción de tratamiento para los pacientes que esperan donantes. Pero solo tienen entre un 40 y un 50 por ciento de posibilidades de sobrevivir unos cinco años. En comparación con más del 80 por ciento de los pacientes que reciben un trasplante de riñón. El costo del tratamiento de diálisis esos cinco años es aproximadamente 10 veces mayor que el de un trasplante. Más de 2 millones de pacientes en todo el mundo que padecen insuficiencia renal clínicamente diagnosticada enfrentan la misma escasez de riñones de donantes. Es casi seguro que el número de casos no diagnosticados sea mucho mayor.
Xenotransplantes la esperanza
El Dr. Winfred Williams, jefe asociado de la división de nefrología del Mass General, sostiene que una nueva fuente de riñones podría resolver un problema persistente en el campo de los trasplantes: el acceso insuficiente de los pacientes de minorías a los trasplantes de riñón. Durante décadas, el xenotrasplante, es decir, la implantación de un órgano animal en un ser humano se ha propuesto como una solución potencial para hacer los riñones más accesibles. Sin embargo, el sistema inmunitario humano rechaza el tejido extraño, lo que puede provocar complicaciones potencialmente mortales.
En los últimos años, los avances científicos como la edición de genes y la clonación han acercado los xenotrasplantes a la realidad. Estos avances permiten modificar genes animales para que los órganos sean más compatibles y menos susceptibles de ser rechazados por el sistema inmunitario.
Los intentos más recientes de xenotrasplante se han realizado con cerdos modificados para que sus órganos sean más parecidos a los humanos. Lo que aumenta la esperanza de que algún día puedan ayudar a paliar la escasez de órganos donados. Los cerdos han sido utilizados en medicina humana durante mucho tiempo, por ejemplo, para injertos de piel o implantes de válvulas cardíacas. Pero trasplantar órganos enteros es mucho más complejo que utilizar tejidos muy procesados.
Precedentes
En septiembre de 2021, cirujanos de la NYU Langone Health de Nueva York realizaron un hito al trasplantar un riñón de cerdo modificado genéticamente a un hombre con muerte cerebral. Poco después, científicos de la Universidad de Alabama en Birmingham anunciaron que habían realizado un procedimiento similar con los mismos resultados.
Cirujanos de la Universidad de Maryland trasplantaron corazones de cerdos modificados genéticamente a pacientes con enfermedades cardíacas en dos ocasiones. Aunque los órganos funcionaron y el primero no pareció ser rechazado, ambos pacientes, que padecían una enfermedad avanzada, murieron poco después.
Según un artículo publicado en Nature, eGenesis, logró trasplantar con éxito riñones de cerdos genéticamente modificados a monos. Los que sobrevivieron una media de 176 días y, en un caso, durante más de dos años. eGenesis es la empresa que proporcionó el órgano para el transplante de Slayman, primera vez que un riñón de cerdo modificado genéticamente se trasplanta a una persona viva.
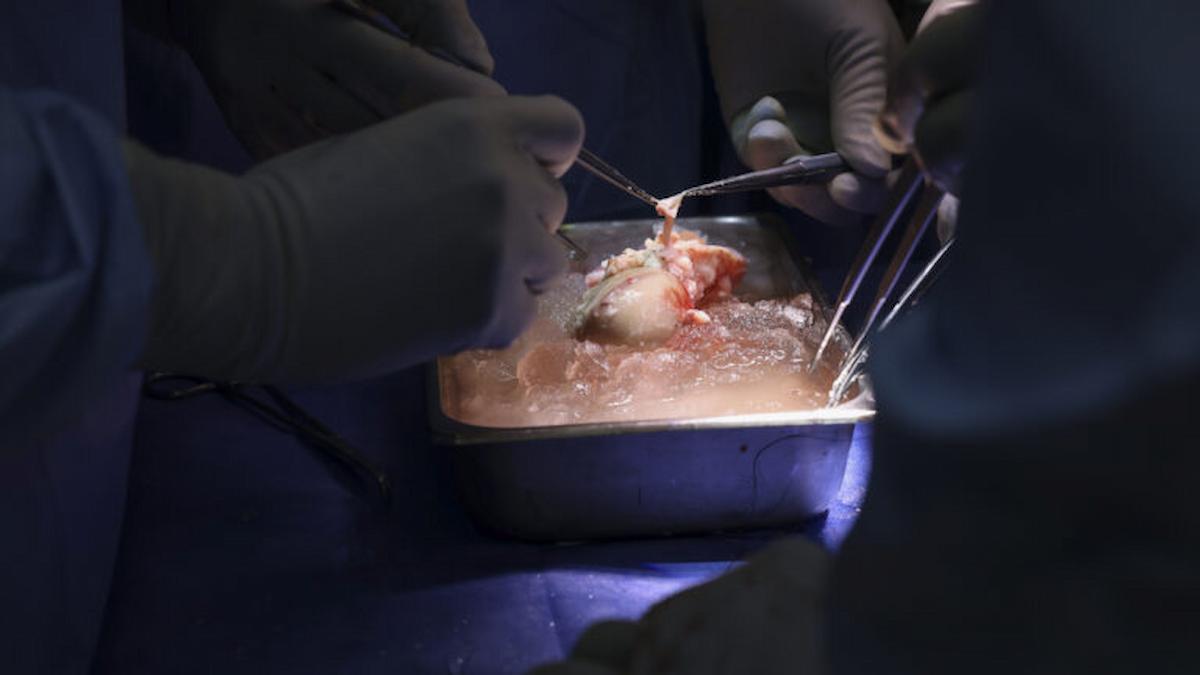
El cerdo fue editado genéticamente para eliminar tres genes implicados en el posible rechazo del órgano. Además, se insertaron siete genes humanos para mejorar la compatibilidad humana. Los cerdos son portadores de retrovirus que pueden infectar a los humanos, y la empresa también inactivó estos patógenos. Según el Dr. Leonardo V. Riella, director médico de trasplantes renales del Mass General, si los riñones de animales modificados genéticamente pueden trasplantarse a gran escala, la diálisis “quedará obsoleta”.

Retos éticos
El Dr. Parsia Vagefi, jefe de trasplantes quirúrgicos del UT Southwestern Medical Center, califica el reciente trasplante de riñón de cerdo a humano como un “gran paso adelante”. Sin embargo, reconoce que se necesitarán estudios con más pacientes en diferentes centros médicos para que el procedimiento esté más ampliamente disponible.
El avance en xenotrasplantes no ha estado exento de críticas. Kathy Guillermo, vicepresidenta senior de People for the Ethical Treatment of Animals, manifestó su preocupación por la explotación de los animales y el riesgo de introducir nuevos patógenos en las poblaciones humanas.
«Utilizar cerdos como fuente de piezas de repuesto es peligroso para los pacientes humanos, mortal para los animales y puede provocar la próxima pandemia. Es imposible eliminar, o incluso identificar, todos los virus que portan los cerdos. Los investigadores deben centrarse en limpiar el sistema de donación de órganos y dejar tranquilos a los animales».
Kathy Guillermo, vicepresidenta senior de People for the Ethical Treatment of Animals
Faltan más
El Dr. Robert Montgomery, director del Instituto de Trasplantes Langone de la Universidad de Nueva York (NYU), en cambio, ve el avance como un paso hacia la creación de una fuente alternativa de órganos para los cientos de miles de personas que padecen insuficiencia renal.
Pero el trasplante seguro de órganos de animales a humanos requiere múltiples pasos para minimizar el riesgo de rechazo del nuevo órgano por parte del sistema inmunitario del receptor y para prevenir infecciones y otras complicaciones. Joren Madsen, catedrático de cirugía Paul S. Russell/Warner-Lambert del HMS y director del Centro de Trasplantes del MGH, afirma que la barrera para el xenotrasplante porcino es formidable, pero que se ha podido superar.
Leonardo Riella, catedrático asociado de cirugía de HMS, afirma que para comprender plenamente la eficacia del trasplante de riñón porcino se requiere no sólo más tiempo, sino también más pacientes. Aunque los resultados a largo plazo del trasplante aún no están claros, hay muchas esperanzas puestas en el potencial del xenotrasplante renal para salvar y mejorar la calidad de vida de los pacientes reduciendo la necesidad de diálisis renal.
Potencial enorme
Dr. Thomas Solbach explica que los trasplantes de riñón son sólo un área de alto perfil donde los xenotrasplantes tienen el potencial de usarse con diversas ventajas para una amplia gama de trastornos, siempre que la práctica clínica esté estrictamente regulada. En el futuro previsible, a medida que continúen los avances en los xenotrasplantes, los órganos animales podrían estar disponibles de forma electiva, incluso con poca antelación.
Podría incluir a pacientes “límite” o actualmente no elegibles, evitando al mismo tiempo barreras culturales a la donación de órganos de personas fallecidas en países como Japón. Un aumento de los xenotrasplantes también ayudaría a reducir el tráfico ilegal de órganos humanos y la incidencia de complicaciones potencialmente mortales derivadas de la donación de seres humanos vivos.
La disponibilidad de órganos animales sólidos podría aumentar significativamente al incluir a los pacientes con tumores sin metástasis. Otra área prometedora son los avances tecnológicos en el trasplante de tejido porcino. Que podrían permitir a los pacientes diabéticos recibir nuevas células de los islotes pancreáticos. De manera similar, las córneas de cerdo podrían usarse en operaciones oculares o células neuronales de cerdos para tratar la enfermedad de Parkinson y la enfermedad de Huntington.
Desafíos por delante
Los trasplantes de órganos, células y tejidos de animales a humanos están destinados a generar controversia por su naturaleza. Para Solbach la enorme velocidad con la que los xenotrasplantes podrían incorporarse a la atención sanitaria clínica convencional en los próximos años significa que los reguladores y las empresas de apoyo deben empezar a pensar ahora en los principales desafíos legales, éticos y operativos que se avecinan en el camino.
Desafíos que incluyen la identificación de las modificaciones genéticas más efectivas para minimizar o eliminar aún más el rechazo de xenoinjertos. También minimizar el riesgo de complicaciones, especialmente infecciones zoonóticas e identificar los mejores regímenes médicos de apoyo para proteger al paciente.
Nuevo marco regulatorio
Actualmente, países como Estados Unidos, Japón y el Reino Unido tienen regulaciones específicas sobre productos xenogénicos y basados en células. China, a pesar de los avances significativos en el desarrollo de cerdos genéticamente modificados para la cirugía de trasplante, aún tiene que desarrollar sus propias regulaciones.
A nivel regional, la UE tiene su propio conjunto de regulaciones sobre xenotrasplantes, mientras que, a nivel mundial, la OMS recomienda que los estados miembros desarrollen sus regulaciones nacionales efectivas antes de permitir los trasplantes de animales a humanos. Sin embargo, los gobiernos y reguladores están luchando por seguir el ritmo de la velocidad a la que se está acelerando la ciencia y la práctica de los xenotrasplantes.
En medio de avances clínicos significativos, es probable que en los próximos años surja un panorama regulatorio global más favorable para los xenotrasplantes. Los eventos que ocupan titulares, como las operaciones en Estados Unidos, y un flujo cada vez mayor de investigaciones innovadoras sobre el tema, están generando debate sobre enigmas regulatorios y de propiedad intelectual. Incluyen desde las reglas de cría de animales hasta la asignación de órganos editados genéticamente a los pacientes antes de que exista la producción a gran escala.
Una luz
Solo en el MGH, hay más de 1.400 pacientes en lista de espera para un trasplante de riñón. Algunos, por desgracia, morirán o enfermarán demasiado para ser trasplantados debido al largo tiempo de espera. La esperanza es que el xenotrasplante se convierta en una opción razonable, ya sea como puente en el camino hacia la recepción de un riñón humano o, con suerte, en el futuro como tratamiento permanente. Aunque hay aspectos éticos que debatir y desafíos médicos por superar.
Los xenotrasplantes podrían ayudar a reducir las disparidades sanitarias asociadas a la insuficiencia y el trasplante de órganos. El acceso desigual de los pacientes de minorías étnicas a los trasplantes de riñón es uno de los problemas más difíciles de resolver en este campo. Las iniciativas políticas sólo han tenido un éxito limitado en 30 años. Sin embargo, un suministro abundante de órganos resultante del actual avence tecnológico podría contribuir en gran medida a lograr la equidad sanitaria. Y ofrecer la mejor solución a la insuficiencia renal: un riñón que funcione bien para todos los pacientes que lo necesiten.
«El éxito de este trasplante es la culminación de los esfuerzos de miles de científicos y médicos a lo largo de varias décadas. Tenemos el privilegio de haber desempeñado un papel importante en este hito. Nuestra esperanza es que este enfoque de trasplante ofrezca un salvavidas a millones de pacientes en todo el mundo que sufren de insuficiencia renal».
Tatsuo Kawai, profesor de cirugía de HMS y director del Centro Legorreta de Tolerancia Clínica al Trasplante en Mass General








